Kyselina salicylová
| Strukturní vzorec | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
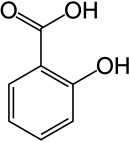
| ||||||||||||||||||||||
| Všeobecné | ||||||||||||||||||||||
| Příjmení | Kyselina salicylová | |||||||||||||||||||||
| ostatní jména | ||||||||||||||||||||||
| Molekulární vzorec | C 7 H 6 O 3 | |||||||||||||||||||||
| Stručný popis |
bezbarvé a bez zápachu, škrábání, sladkokyselé chuťové krystaly s nepříjemnou pachutí |
|||||||||||||||||||||
| Externí identifikátory / databáze | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Informace o drogách | ||||||||||||||||||||||
| ATC kód | ||||||||||||||||||||||
| vlastnosti | ||||||||||||||||||||||
| Molární hmotnost | 138,12 g mol -1 | |||||||||||||||||||||
| Fyzický stav |
pevně |
|||||||||||||||||||||
| hustota |
1,44 g cm −3 |
|||||||||||||||||||||
| Bod tání |
159 ° C |
|||||||||||||||||||||
| bod varu |
211 ° C (27 hPa ) |
|||||||||||||||||||||
| Hodnota p K S. |
|
|||||||||||||||||||||
| rozpustnost |
|
|||||||||||||||||||||
| bezpečnostní instrukce | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologické údaje |
|
|||||||||||||||||||||
| Kdekoli je to možné a obvyklé, používají se jednotky SI . Pokud není uvedeno jinak, uvedené údaje platí pro standardní podmínky . | ||||||||||||||||||||||
Kyselina salicylová ( kyselina o- hydroxybenzoová) je chemická látka s antipyretickými a analgetickými účinky. Kyselina salicylová se vyskytuje ve formě svého methylesteru v éterických olejích a jako rostlinný hormon v listech , květech a kořenech různých rostlin a je důležitá pro obranu rostliny před patogeny . Dostalo své jméno, protože se dříve získávalo primárně oxidačním zpracováním salicinu , který je obsažen v kůře různých vrb (vědecky Salix spec. ).
Je také známá pod názvem kyselina spirová , protože ji lze získat ze šťávy vrabčího keře ( tužebník ). Z názvu Spirsäure také značkové odvozuje aspirin pro kyseliny acetylsalicylové z: A cetyl SPIR kyseliny. Soli kyseliny salicylové se nazývají salicyláty .
Raffaele Piria nejprve izolovala kyselinu salicylovou ze salicinu (1838).
Výskyt a těžba
biosyntéza
Kyselina salicylová se nachází ve velkém počtu rostlin a působí zde jako fytohormon . Existují dvě rozčleněné dráhy biosyntézy: fenylpropanoidová cesta v cytoplazmě vycházející z fenylalaninu a izochorismátová cesta v chloroplastech. Většina kyseliny salicylové je methylována jako kapalný methylsalicylát , aby byla účinná jako těkavý derivát pro dálkovou přepravu. U rostlin tabáku a Arabidopsis thaliana se ukázalo, že tato forma je důležitá pro systémově získanou rezistenci. Kromě toho může být kyselina salicylová glykosylována a skladována ve vakuolách jako neaktivní forma.
Technická výroba
Technicky se vyrábí z oxidu uhličitého a fenolátu sodného pomocí Kolbe-Schmittovy reakce (označované také jednoduše jako syntéza kyseliny salicylové) . Tato umělá výroba do značné míry nahradila těžbu z vrbové kůry.
Již v roce 1874 byla na základě myšlenky Hermanna Kolbeho převedena syntéza kyseliny salicylové z laboratoře do tovární výroby, kde provozoval továrnu na kyselinu salicylovou Dr. Schmitt Friedrich von Heyden Dr. F. von Heyden v Drážďanech, který se o rok později přestěhoval do Radebeulu . Odtamtud byla kyselina salicylová prodávána jako první průmyslově vyráběná a „balená“ droga na světě. Friedrich von Heyden je považován za zakladatele průmyslové výroby kyseliny salicylové ve farmaceutickém průmyslu.
Chemicko-fyzikální vlastnosti
Kyselina salicylová je jednou z aromatických látek díky benzenovému kruhu, který obsahuje . Jelikož obsahuje karboxylovou a hydroxylovou skupinu , patří k hydroxykarboxylovým kyselinám . Kvůli p-stabilitě karboxylové skupiny vůči hydroxylové skupině ji lze také označit jako p-hydroxykarboxylovou kyselinu. Jelikož je hydroxylová skupina vázána přímo na aromatický benzenový kruh, patří také k fenolům, a tedy také k fenolickým kyselinám .
Při rychlém a intenzivním zahřívání dekarboxyláty kyseliny salicylové tvoří fenol . Při teplotě nad 76 ° C látka částečně sublimuje a z chladících par se tvoří krystaly ve tvaru jehly .
Vysoká kyselost - ve srovnání s jinými hydroxybenzoovými kyselinami - je způsobena stabilizací salicylátového aniontu prostřednictvím vodíkové vazby se sousední hydroxyskupinou.
Analytické důkazy: Protože kyselina salicylová je formálně enol (v tomto případě fenol ) kyseliny β-ketokarboxylové, tvoří s roztokem chloridu železitého fialový komplex, komplex tris-salicylát železitý:
Tento důkaz není konkrétní, protože sloučeniny podobné esterům acetoctové mají stejnou reakci. Bod vzplanutí je 157 ° C a teplota vznícení je 570 ° C,
Biologická funkce
Jako fytohormon hraje kyselina salicylová důležitou roli jako regulační signál při abiotickém stresu, jako je sucho a teplo, chlad nebo osmotický tlak. Kromě toho je pro rostlinu důležitý při obraně proti patogenům, je exprimován lokálně i systémově v případě napadení a je schopen modulovat genovou expresi. Existují také důkazy, že kyselina salicylová hraje roli v růstu a vývoji rostliny.
použití
Kyselina salicylová se používá při výrobě barviv a vůní a kyselina acetylsalicylová (ASA, známá také pod značkou Aspirin ), která se používá jako lék proti bolesti, protizánětlivý a antikoagulační lék . Ve formě nerozpustného subsalicylátu vizmutu se používá proti průjmům a poruchám gastrointestinálního traktu.
Kyselina salicylová se také používá jako tavidlo při měkkém pájení .
Kyselina salicylová má antimikrobiální účinek, ale její použití jako konzervační látky v potravinách je zakázáno. V kosmetice je povolena kyselina salicylová v souladu s nařízením (ES) č. 1223/2009 o kosmetických prostředcích jako prostředek proti lupům v prostředcích na mytí vlasů do maximálně 3%, u jiných prostředků do koncentrace 2% a při použití jako konzervační prostředek až do maxima 0,5%. V léčivých přípravků , kyselina salicylová od 5% roztok vykazuje A kerato - a tedy i comedolytic účinkem , které je dostatečné pro léčení akné . V 10% roztoku se používá k ošetření kuřích , bradavic a kožních hub .
nežádoucí účinky
Vedlejší účinky farmakoterapie
Kyselina salicylová je metabolit kyseliny acetylsalicylové, která se v těle rychle hydrolyzuje . Nežádoucími účinky jsou zejména alergické reakce , sklon ke krvácení, bronchokonstrikce ( bronchiální astma ), poškození žaludeční sliznice s krvácením, v jednotlivých případech poškození jater. Rovněž byla pozorována retence kyseliny močové, hyperurikémie a poškození ledvin. Důležitou metabolickou cestou v játrech je přeměna na kyselinu salicylurovou .
toxicita
Kyselina salicylová na kůži, sliznicích a očích akutně dráždí poškození tkáně. Navíc, když se užívá orálně nebo jiným způsobem, kyselina způsobuje tlumení dýchacího centra a narušení důležitých metabolických procesů a centrálního nervového systému . Při chronické expozici se projeví poruchy gastrointestinálního traktu. V pokusech na zvířatech ukázalo orální a dermální podání kyseliny salicylové různé účinky na zvířata (kočky, myši, králíky a krysy), jako je ospalost, svalová slabost a poškození orgánů jater a ledvin. Akutní toxicita LD 50 byla u potkanů mezi 400 a 1300 mg / kg orálně a 2 g / kg dermálně. U lidí byly po dermálním podání stanoveny hodnoty TD Lo 57 až 111 mg / kg. Plazmatický poločas salicylové kyseliny je přibližně 2 až 3 hodiny.
bezpečnostní instrukce
Na návrh společnosti Novacyl byla v letech 2015 a 2016 revidována chemická klasifikace kyseliny salicylové. Výbor pro posuzování rizik (RAC) od Evropské agentury pro chemické látky (ECHA) změnila klasifikaci pro kyselinu salicylovou takto dne 10. března 2016: kyselina salicylová je klasifikován jako reprodukční toxický Repr 2, jakož i Acut Tox 4 a Eye Dam 1. Varovná upozornění byla nastavena na H361d, H302 a H318. Tuto klasifikaci RAC musí Evropská komise v platných právních předpisech ještě provést, ale jejím zveřejněním představuje stav znalostí, který musí společnosti a úřady zohlednit.
Deriváty kyseliny salicylové
Solí
Kyselina salicylová reaguje s hydroxidem sodným za vzniku salicylátu sodného .
Ester
Pokud kyselina salicylová reaguje s alkoholem , vznikne za vyloučení vody ester karboxylové kyseliny nebo ester kyseliny salicylové . Může také tvořit estery s organickými kyselinami , v takovém případě potom při reakci funguje jako alkohol. Estery kyseliny salicylové se používají hlavně v kosmetickém a parfémovém průmyslu jako antirevmatická činidla v přísadách do koupele, mastích nebo krémech a také jako vůně a UV filtry v opalovacích krémech. Nejznámějším esterem kyseliny salicylové je kyselina acetylsalicylová . Zde hydroxylovou skupinu ze salicylové kyseliny se esterifikuje s karboxylovou skupinou z octové kyseliny. Další příslušné estery kyseliny salicylové jsou methylsalicylát , ethylsalicylát , benzylsalicylát , isobutylsalicylát , isopentylsalicylát , fenylsalicylát a hydroxyethylsalicylát .
Halogenové deriváty
Tím, bromace s elementárním bromem v ledové kyselině octové , kyseliny 3,5-dibromosalicylic se vytvoří se sůl mědi, které se používá jako fungicid a baktericid .
Biochemicky relevantní kyselina 3,5-diiodosalicylic se získá podle jodací s chloridem jodu . Deriváty kyseliny salicylové halogenované v poloze 4, jako je kyselina 4-jodosalicylová , nelze získat přímo.
literatura
- F. von Heyden: kyselina salicylová . In: Altán . Vydání 10, 1863, str. 172 ( plný text [ Wikisource ]).
- Beilsteinův manuál . Svazek 10, Textarchiv - internetový archiv (o kyselině salicylové a jejích derivátech, literatura zaznamenaná až do roku 1910).
webové odkazy
Individuální důkazy
- ↑ Záznam o KYSELINĚ SALICYLOVÉ v databázi CosIng Evropské komise, přístup ke dni 14. ledna 2020.
- ↑ Vstup na kyselinu salicylovou. In: Römpp Online . Georg Thieme Verlag, přístup 1. června 2014.
- ↑ b c d e f g h i vstup na kyselinu salicylovou v databázi GESTIS látkové v IFA , přístupné 14. ledna 2020. (Vyžadován JavaScript)
- ↑ a b CRC Handbook of Tables for Organic Compound Identification . Třetí vydání, 1984, ISBN 0-8493-0303-6 .
- ^ Claudia Synowietz, Klaus Schäfer (eds.): Chemický kalendář. 3. Vydání. Springer, Berlin / Heidelberg / New York / Tokyo 1984, ISBN 3-540-12652-X .
- ↑ Vstup na kyselinu salicylovou v seznamu klasifikací a označení všech v Evropské agentury pro chemické látky (ECHA), přístupné ze dne 30. prosince 2019. Výrobci a distributoři mohou rozšířit do harmonizované klasifikace a označování .
- ↑ a b c Příručka toxikologie. 4 svazky, WB Saunders Co., Philadelphia 1956-1959; Svazek 5, 1959, s. 148.
- ↑ a b Drogy v Japonsku. Svazek 6, 1982, s. 291.
- ↑ a b BIOFAX. Industrial Bio-Test Laboratories Inc., datové listy. Svazek 21-3 / 1971.
- ↑ a b Údaje o akutní toxicitě. Journal of the American College of Toxicology, Part B. Volume 15 (Suppl.)
- ↑ a b P. A. Soyka, LF Soyka: Absorpce kyseliny salicylové . In: Journal of the American Medical Association . páska 244 , č. 7 , 1980, str. 660-661 , PMID 7392165 (anglicky, pmj.bmj.com [PDF]).
- ↑ a b C. M. Dwyer, RH McCloskey, RE Kerr: Otrava topickou kyselinou salicylovou. In: Postgraduální lékařský deník . páska 70 , č. 820 , 1994, str. 146 , PMID 8170891 , PMC 2397637 (plný text).
- ^ Doris Schwarzmann-Schafhauser: kyselina salicylová. In: Werner E. Gerabek a kol. (Ed.): Encyclopedia Medical History. De Gruyter, Berlín / New York 2005, ISBN 3-11-015714-4 , s. 1282.
- ↑ Například Salix alba , Filipendula (Spirea) ulmaria a čajové bobule (Gautheria procumbens).
- ↑ a b M. Rivas-San Vicente, J. Plasencia: Kyselina salicylová mimo obranu: její role v růstu a vývoji rostlin . In: Journal of Experimental Botany . páska 62 , č. 10 , 1. června 2011, s. 3321-3338 , doi : 10.1093 / jxb / err031 .
- ↑ Specifikace patentu (německý patent DE4415527) na použití kyseliny salicylové nebo kyseliny acetylsalicylové při měkkém pájení.
- ↑ AA Hartmann: Vliv různých faktorů na lidskou pleťovou flóru . In: Semináře z dermatologie . páska 9 , č. 4 , 1990, str. 305-308 , PMID 2285575 .
- ↑ Kyselina salicylová jako konzervační látka pro spotřební zboží. Jejich hodnota, užitečnost a neškodnost, odůvodněná úsudkem znalých orgánů a soudními znalostmi. Chemická továrna von Heyden, Radebeul-Dresden 1896 urn : nbn: de: hbz: 061: 2-11219 .
- ↑ Doris Fanta, Christine Messeritsch-Fanta: Akné 1999. Stále potřebujeme dermatologa? In: Dermatolog . páska 50 , č. December 12 , 1999, str. 900-911 , doi : 10,1007 / s001050051009 .
- ↑ AW Frahm, HHJ Hager, F. v. Bruchhausen, M. Albinus, H. Hager: Hager's Handbook of Pharmaceutical Practice: Volume 4: Substances AK. Birkhäuser, 1999, ISBN 978-3-540-52688-9 , s. 42.
- ↑ Odborné informace Aspirin® 100 mg tablety ( Memento ze dne 29. dubna 2006 v internetovém archivu ; PDF).
- ^ Rozhodnutí RAC ze dne 10. března 2016
- ↑ US Patent 399034: Biocidní soli kyseliny 3,5-dibromosalicylové .








