Sublimace (fázový přechod)
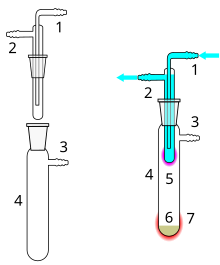
1 přívodu chladicí vody
2 chladicí vody výpusť
3 Připojení vakua
4 Sublimace komoru
5 sublimovaný materiál
6 Unsublimated materiál
7 vnější tepelný příkon
Jako sublimace vzácně sublimace (z latinského sublimatio nebo sublimare , dříve ve smyslu „čistit destilací, chemicky čistá, jak je to možné reprezentovat“ z sublimis „high vzduchu ušlechtilou“), je proces okamžitého přechodu na látky podaná pevný do plynného stavu agregace bez předchozího zkapalnění. Jedná se o čistě fyzikální proces, při kterém látka zůstává chemicky nezměněna.
Za tlakových a teplotních podmínek, za kterých dochází k sublimaci, neexistuje stav kapalného agregátu, jak je vidět na fázovém diagramu vpravo. Tyto podmínky se také označují jako sublimační tlak a sublimační teplota, nebo se berou společně jako sublimační bod . To je zase součástí sublimační křivky fázového diagramu, která je v sousedním příkladu dána fázovou hraniční čárou mezi pevnou látkou a plynem pod trojným bodem .
Fázová změna v opačném směru než sublimace je odborně označována jako resublimace nebo také jako depozice nebo desublimace. Bod resublimace čistých látek je shodný s bodem sublimace. V případě směsí je třeba poznamenat, že oba se mohou lišit, a proto také v tomto případě hraje roli směr fázového přechodu .
Pokud existuje sublimační teplota za normálního tlaku, nazývá se to normální sublimační teplota a látka je uvedena do tabulky se svou hodnotou, aniž by byl dodatečně specifikován sublimační tlak.
Každá látka absorbuje tzv sublimační entalpie při jeho sublimace , což se rovná součtu z entalpie tání a entalpie odpařování .
Příklady
- Sublimace ve skutečném smyslu
- Bor , uhlík a arsen , ale také organické sloučeniny, jako je kafr, se při zahřívání za normálního tlaku převádějí přímo do plynné podoby.
- Suchý led , v -78.5 ° C zmrzlé oxidu uhličitého se sublimuje při tepelném a přímo vstupuje do plynného skupenství výše. Za normálních tlakových podmínek žádná kapalina jako např B. při ohřevu vodního ledu : zde je odvozen termín suchý led .
- Sublimace nad trojným bodem
- Pokud je vzduch za atmosférického tlaku dostatečně studený a suchý , přechází voda také přímo ze svého pevného agregačního stavu do plynné formy ( vodní pára ). Důvodem je to, že tlak vodní páry je parciální tlak vzduchu, a je proto nižší než atmosférický tlak vzduchu. Tento fázový přechod proto probíhá ve fázovém diagramu pro vodu v sublimační oblasti pod trojným bodem, i když se zdá, že k tomu dochází za atmosférického tlaku. Díky tomuto efektu vlhké prádlo schne ve venkovním vzduchu za odpovídajících podmínek v mrazivých podmínkách rychleji než ve vnitřních místnostech, jejichž teplejší vzduch je již víceméně nasycen vodní párou.
- Jód sublimuje za normálního tlaku při zahřívání, čímž je zvláště účinný jako fialový plyn, a proto se často používá jako ukázkový experiment. Ve skutečnosti je tlak v trojitém bodě (386,65 K, 12,1 kPa) hluboko pod okolním tlakem (101,315 kPa). Dokud je však teplota udržována pod bodem tání (113,70 ° C), jód se ve skutečnosti mění z pevného na plynný stav. Jód se navíc nejprve roztaví do sytě purpurové až černé kapaliny.
Zmatek s disociací
Sublimaci lze zaměňovat s disociací . Například chlorid amonný se při zahřívání rozpadá na amoniak a chlorovodík .
použití
Při zpracování materiálů pomocí sublimačního řezání laserovým paprskem dochází k sublimaci s vysokým pulzním výkonem laseru. Materiál se nejprve neroztaví, ale přechází přímo z pevného do plynného stavu. Výsledkem je velmi čistý řez bez strusky nebo roztřepených okrajů.
Další aplikace jsou lyofilizace potravin, která je velmi šetrná ve srovnání s jinými způsoby sušení, a sublimační tisk .
Sublimace je také alternativou k rekrystalizaci při čištění produktů v syntetické chemii. Ve srovnání s krystalizací nabízí sublimace několik výhod: Produkty jsou často velmi čisté a dokonce i ta nejmenší množství lze pohodlně sublimovat v sublimačním zařízení. Autoři uvádějí příklad uplatnění sublimaci malých množstvích v radiochemické pole pro radiochemické purifikace nuklidu v souvislosti se stanovením poločasem z 79 Se . Sublimace je především laboratorní proces čištění tkanin, např. B. pro ferocen a pyrogallol . Nevýhodou ve srovnání s krystalizací z taveniny je poměrně obtížné zvětšování během sublimace. V chemickém průmyslu má proto technická implementace sublimace jako separační metody pouze druhotný význam. Sublimace se používá průmyslově jako rafinace pro naftalenu , anhydrid kyseliny ftalové , kafr , antrachinon , kyselina salicylová , kyselina benzoová , hexafluoridu uranu a mnoho kovů.
Transportní reakce
Chemické transportní reakce se používají k čištění látek (většinou kovů) pomocí sublimace. Zde se však látka, která má být čištěna, v chemických reakcích nejprve převede na sekundární látku, která z. B. má nižší sublimační tlak. Příklady transportních reakcí jsou Mondův proces nebo Van-Arkel-de-Boerův proces .
Viz také
Individuální důkazy
- ^ Wilhelm Hassenstein, Hermann Virl : Kniha ohňostrojů z roku 1420. 600 let německých práškových zbraní a puškařství. Dotisk prvního tisku z roku 1529 s překladem do vysoké němčiny a vysvětlením od Wilhelma Hassensteina. Verlag der Deutsche Technik, Mnichov 1941, s. 40 ( sublimace ).
- ↑ Vstup na sublimaci . In: Kompendium chemické terminologie IUPAC („zlatá kniha“) . doi : 10,1351 / goldbook.S06069 .
- ^ Michael Wächter: Chemielabor-Úvod do laboratorní praxe , Wiley-VCH Verlag, Weinheim, 1. vydání, 2011, s. 76, ISBN 978-3-527-32996-0 .
- ↑ jom: JEN SE Zeptat!: Odpařená ledová . In: badische-zeitung.de, Ratgeber, Bildung & Wissen, 10. prosince 2011 (16. prosince 2011).
- ↑ NileRed: Jódový mýtus. Citováno 13. září 2017 . Tání a tmavě purpurová barva tekutého jódu jsou jasně viditelné.
- ^ Heinz GO Becker et al.: Organikum , Johann Ambrosius Barth Verlag Leipzig, Berlin, Heidelberg, s. 53–54, ISBN 3-335-00343-8 .
- ↑ Physikalisch-Technische Bundesanstalt: Poločas rozpadu 79 Se , News 2010.
- ↑ Jörg, G., Bühnemann, R., Hollas, S., Kivel, N., Kossert, K., Van Winckel, S., Lierse v. Gostomski, Ch. Applied Radiation and Isotopes 68 (2010), 2339-2351.
- ^ TJ Kealy, PL Pauson: Nový typ organo -železné sloučeniny . Nature 1951, 168, 1039. doi : 10,1038 / 1681039b0 .
- ↑ Otto-Albrecht Neumüller (Ed.): Römpps Chemie-Lexikon. Svazek 5: Pl-S. 8. přepracované a rozšířené vydání. Franckh'sche Verlagshandlung, Stuttgart 1987, ISBN 3-440-04515-3 .


