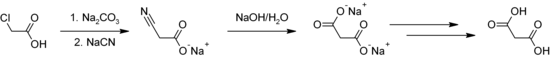Malonová kyselina
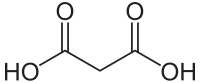
| Strukturní vzorec | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||
| Všeobecné | ||||||||||||||||||||||
| Příjmení | Malonová kyselina | |||||||||||||||||||||
| ostatní jména |
|
|||||||||||||||||||||
| Molekulární vzorec | C 3 H 4 O 4 | |||||||||||||||||||||
| Stručný popis |
bezbarvé krystaly |
|||||||||||||||||||||
| Externí identifikátory / databáze | ||||||||||||||||||||||
| ||||||||||||||||||||||
| vlastnosti | ||||||||||||||||||||||
| Molární hmotnost | 104,06 g mol −1 | |||||||||||||||||||||
| Fyzický stav |
pevný |
|||||||||||||||||||||
| hustota |
1,60 g cm −3 |
|||||||||||||||||||||
| Bod tání | ||||||||||||||||||||||
| bod varu |
Rozklad od 140 ° C |
|||||||||||||||||||||
| Tlak páry |
0,1 Pa (18,5 ° C) |
|||||||||||||||||||||
| p K S hodnota |
|
|||||||||||||||||||||
| rozpustnost |
|
|||||||||||||||||||||
| bezpečnostní instrukce | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologická data | ||||||||||||||||||||||
| Pokud je to možné a obvyklé, používají se jednotky SI . Pokud není uvedeno jinak, uvedené údaje platí pro standardní podmínky . | ||||||||||||||||||||||
Kyselina malonová (propandiová kyselina ) je dikarboxylová kyselina , která je krystalická při teplotě místnosti, a jehož estery a soli se nazývají malonáty (např. Diethyl-malonát = diethyl- malonát ).
Historie a výskyt
Kyselina malonová byl objeven v roce 1858 při oxidaci z kyseliny jablečné . Název je odvozen z latinského malum = jablko (rod rostlin). Kyselina malonová se nachází ve šťávě z cukrové řepy . Kyselina malonová je buňka toxin , který inhibuje na citrát cyklus ( Krebsův cyklus ) inhibicí sukcinátdehydrogenázy .
Prezentace a extrakce
Kyselina malonová se vyrábí mimo jiné reakcí kyseliny chloroctové s kyanidem sodným (NaCN) ( syntéza Kolbeho nitrilu ) a následnou hydrolýzou výsledné kyseliny kyanooctové .
vlastnosti
Kyselina malonová vytváří krystaly bez barvy a zápachu, které mají teplotu tání 136 ° C a snadno se rozpouštějí ve vodě. Sloučenina se vyskytuje ve třech polymorfních krystalových formách. Forma γ existuje pouze při nízkých teplotách a mění se na formu β při −225,9 ° C. Fázový přechod z β formy do α formy probíhá při 79 ° C. Formy α a β nebo β a γ jsou navzájem enantiotropní . Pevná látka se rozkládá nad bodem tání s eliminací oxidu uhličitého za vzniku kyseliny octové . Tato dekarboxylace probíhá od 70 ° C ve vodném roztoku . Ve rozpouštědlech s vyšším bodem varu, jako je ethylenglykol , trimethylenglykol , 1,3-butandiol a 2,3-butandiol , reakce probíhá při reakci vyšší než 100 ° C jako reakce prvního řádu .
Pokud se kyselina malonová zahřívá se silně dehydratačními činidly, např. B. s oxidem fosforečným vede intramolekulární dehydratace ke špatným výtěžkům suboxidu uhlíku , známého také jako anhydrid kyseliny malónové.
Malonová kyselina je CH-kyselá sloučenina, tzn. To znamená, že proton lze snadno oddělit od centrálního uhlíku v důsledku účinku obou karboxylových skupin odebírajících elektrony .
použití
Deriváty kyseliny malonové jsou syntetické stavební kameny v Knoevenagelově kondenzaci nebo syntéze esteru malónu a používají se například k výrobě kyseliny barbiturové a jejích derivátů . Zejména William Henry Perkin, Jr. poprvé cyklopropanace reakcí diethylesteru CH-kyselé kyseliny malonové s 1,2-dibromethanem a dvěma ekvivalenty ethoxidu sodného. Když se zahřívají směsi cyklických iminů a kyseliny malónové, vytvářejí se beta- aminokarboxylové kyseliny . Do Evropy se ročně dováží 10 až 100 tun.
Malonát: riziko záměny s malátem a maleátem
Malonát se nesmí zaměňovat s kyselinou aniontem kyseliny jablečné , malátové iontu, nebo aniontu z kyseliny maleinové , na maleát .
Individuální důkazy
- ↑ Záznam o MALONICKÉ KYSELINĚ v databázi CosIng Komise EU, přístup 2. července 2020.
- ↑ a b c d e f g Vstup na kyselinu malonovou. In: Römpp Online . Georg Thieme Verlag, přístup 13. června 2014.
- ↑ b c d e f g vstup na malonové kyseliny v databázi GESTIS látkové v IFA , přístupné 10. ledna 2017. (Vyžadován JavaScript)
- ↑ a b chem.wisc.edu: pKa Data , sestavil R. Williams (PDF, 78 kB).
- ↑ Datový list kyseliny malonové od Sigma-Aldrich , přístup 10. srpna 2012 ( PDF ).
- ↑ Nathan Weiner: Kyselina malonová v: Organic Syntheses . 18, 1938, s. 50, doi : 10,15227 / orgsyn.018,0050 ; Sb. Vol.2, 1943, s. 376 ( PDF ).
- ↑ Fukai, M.; Matsuo, T .; Suga, H.: Termodynamické vlastnosti fázových přechodů v kyselině malonové a jejím deuterovaném analogu v Thermochimu. Acta 183 (1991) 215-243, doi : 10,1016 / 0040-6031 (91) 80461-Q .
- ^ Clark, LW: Kinetika dekarboxylace kyseliny malonové a jiných kyselin v neutrálních rozpouštědlech v J. Phys. Chem. 71 (1967) 2597-2601, doi : 10,1021 / j100867a031 .
- ↑ Jürgen Martens, Jürgen Kintscher a Wolfgang Arnold : Syntéza a stereochemie nových 2-substituovaných 4-thiazolidinyloctových kyselin, in: Tetrahedron , 1991 , 47 , pp. 7029-7036, doi : 10,1016 / S0040-4020 (01) 96157- 5 .
- ↑ Kyselina malonová - Informace o látce - ECHA. Citováno 10. května 2018 (britská angličtina).
- ^ William B. Jensen: Původ jmen Malic, Maleic a Malonic Acid , in: J. Chem. Educ. , 2007 , 84 , s. 924, doi : 10,1021 / ed084p924 .